PROSES VALİDASYONU EĞİTİMİ
Proses Validasyonu,
- Tıbbi cihaz endüstrisinde, bir işlemin sonucunun pratik olarak garanti edilebilecek şekilde incelemeye tabi tutulduğunu belirtmek için kullanılan terimdir.
- Bir prosesin validasyonu, bir prosesin belirli limitler dahilinde çalıştırıldığında, önceden belirlenmiş tasarım ve geliştirme gereksinimlerine uygun olarak tutarlı bir şekilde ürün üreteceğini göstermeyi gerektirir.
Bu kapsamda Proses Validasyonu Eğitimi Genel Müdürümüz Gökhan Yalçın tarafından tıbbi cihaz üreticisi firmalarımızın kalite birimi temsilcilerine verildi. Katılımlarından dolayı teşekkür ederiz.
Proses nedir?
Proses, kontrollere tabi olan bir veya daha fazla faaliyettir. Girdileri çıktılara dönüştürmek için kaynakları kullanır.
Prosedür: Bir faaliyeti veya süreci yürütmek için belirtilen yol (belgelenmelidir.)
Validasyon Nedir?
Validasyon bir prosesin doğru ve kesin olarak zaman içinde tutarlı çıktı ürettiğini kanıtlanması için yapılması gereken sistematik bir yöntemdir.
Valide edilmiş yöntemle çalışıldığında yapılan işlemin;
- kesin,
- doğru,
- spesifik,
- tutarlı,
- geçerli
- güvenilir olduğu garanti edilmiş olur.
Proses Validasyon Terminolojisi
Kurulum Kalifikasyonu (IQ):
- Proses ekipmanının ve yardımcı sistem kurulumunun tüm kilit yönlerinin üreticinin onaylı spesifikasyonuna uyduğunu ve ekipman tedarikçisinin tavsiyelerinin uygun şekilde dikkate alındığını nesnel kanıtlarla belirlemek
Operasyonel Kalifikasyonu (OQ):
- Önceden belirlenmiş tüm gereksinimleri karşılayan ürünle sonuçlanan süreç kontrol limitlerini ve eylem seviyelerini nesnel kanıtlarla belirlemek.
Performans Kalifikasyonu (PQ):
- Prosesin, öngörülen koşullar altında tutarlı bir şekilde önceden belirlenmiş tüm gereksinimleri karşılayan bir ürün ürettiğinin nesnel kanıtlarla belirlenmesi.
Proses Validasyonu (Geçerli Kılma):
- Bir sürecin tutarlı bir şekilde önceden belirlenmiş gereksinimleri karşılayan bir sonuç veya ürün ürettiğinin nesnel kanıtlarla onaylanması.
Verifikasyon (Doğrulama):
- İnceleme yoluyla teyit ve belirtilen gerekliliklerin yerine getirildiğine dair nesnel kanıt sağlanması.
Kalifikasyon:
- Bir malzeme, ekipman veya sistemin spesifikasyonlarının tanımlanması ve bu spesifikasyonlara uygunluğunun ölçülmesidir.
Valide edilmesi gereken prosesler
- Sterilizasyon işlemleri
- Temiz oda ortam koşulları
- Aseptik dolum işlemleri
- Steril ambalaj mühürleme işlemleri
- liyofilizasyon işlemi
- Isıl işlem süreçleri
- Kaplama işlemleri
- Plastik enjeksiyon kalıplama işlemleri
Ne zaman Valide Ederiz?
- Proses çıkışı %100 inceleme ve test ile doğrulanamaz
- Proses çıktısı yalnızca tahrip edici testlerle doğrulanabilir
- Süreç iyileştirme ve maliyeti düşürme
Özel veya kritik süreç:
- Sterilizasyon
- Isıl işlem
- Enjeksiyon kalıplama
- Elektro-Kaplama veya cilalama
- Yapıştırma, yapıştırma veya kaynak tertibatları
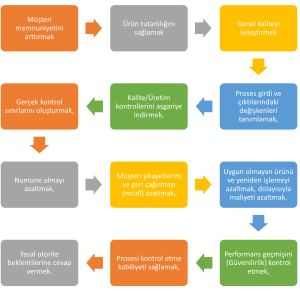
Neden Valide Ediyoruz?
Validasyon Aşamaları
Validasyon ekibi oluşturulduktan sonraki adım, yaklaşımı planlamak ve gereksinimleri tanımlamaktır. Pek çok üretici, valide edilecek prosesleri, validasyonlar için çizelgeyi, validasyon gerektiren prosesler arasındaki karşılıklı ilişkileri ve zamanlamayı tanımlayan bir ana validasyon planını geliştirir.
Bunlar belirlendikten ve doğrulamaların amacı ve kapsamı açıkça belirtildiğinde ve bilindiğinde, protokol geliştirme başlar.
Ürün/süreç gereksinimlerine göre IQ, OQ ve PQ olmak üzere üç aşamanın tümü için:
- Neyin doğrulanacağını/ölçüleceğini belirleyin
- Nasıl doğrulanacağını/ölçüleceğini belirleyin
- Kaç tanesinin doğrulanacağını/ölçüleceğini belirleyin, yani istatistiksel anlamlılık
- Ne zaman doğrulanacağını/ölçüleceğini belirleyin
- Kabul/red kriterlerini tanımlayın
- Gerekli belgeleri tanımlayın
Kurulum Kalifikasyonu (IQ):
- Basitçe söylemek gerekirse, IQ doğru kurulmuş mu? Önemli IQ hususları şunlardır:
- Ekipman tasarım özellikleri (yani inşaat temizlenebilirliği malzemeleri vb.)
- Kurulum koşulları (kablolama, yardımcı programlar, işlevsellik, vb.)
- Kalibrasyon, önleyici bakım, temizlik programları
- Güvenlik özellikleri
- Tedarikçi belgeleri, baskılar, çizimler ve kılavuzlar
- Yazılım dokümantasyonu
- Yedek parça listesi
- Çevresel koşullar (temiz oda gereksinimleri, sıcaklık, nem gibi)
Operasyonel Kalifikasyonu (OQ):
- OQ değerlendirmeleri şunları içerir:
- Proses kontrol limitleri (zaman, sıcaklık, basınç, hat hızı, kurulum koşulları vb.)
- Yazılım parametreleri
- Hammadde özellikleri
- Proses işletim prosedürleri
- Malzeme taşıma gereksinimleri
- Süreç değişikliği kontrolü
- Eğitim
- Sürecin kısa vadeli kararlılığı ve kabiliyeti, (enlem çalışmaları veya kontrol çizelgeleri)
- Potansiyel arıza modları, eylem seviyeleri ve en kötü durum koşulları (Arıza Modu ve Etkileri Analizi, Arıza Ağacı Analizi)
- Anahtar süreç parametrelerini belirlemek için tarama deneyleri ve süreci optimize etmek için istatistiksel olarak tasarlanmış deneyler gibi istatistiksel olarak geçerli tekniklerin kullanımı bu aşamada kullanılabilir.
Performans Kalifikasyonu (PQ):
PQ değerlendirmeleri şunları içerir:
- OQ’da oluşturulan gerçek ürün ve süreç parametreleri ve prosedürleri
- Ürünün kabul edilebilirliği
- OQ’da belirtilen süreç kapasitesinin güvencesi
- Süreç tekrarlanabilirliği, uzun süreli süreç kararlılığı
Sonuç Raporu
Validasyon faaliyetlerinin sonunda bir nihai rapor hazırlanmalıdır. Bu rapor, tüm protokolleri ve sonuçları özetlemeli ve bunlara atıfta bulunmalıdır. Sürecin doğrulama durumu ile ilgili sonuçlar çıkarmalıdır. Nihai rapor, validasyon ekibi ve uygun yönetim tarafından gözden geçirilmeli ve onaylanmalıdır.
Daha fazla bilgi için: Validasyonlar